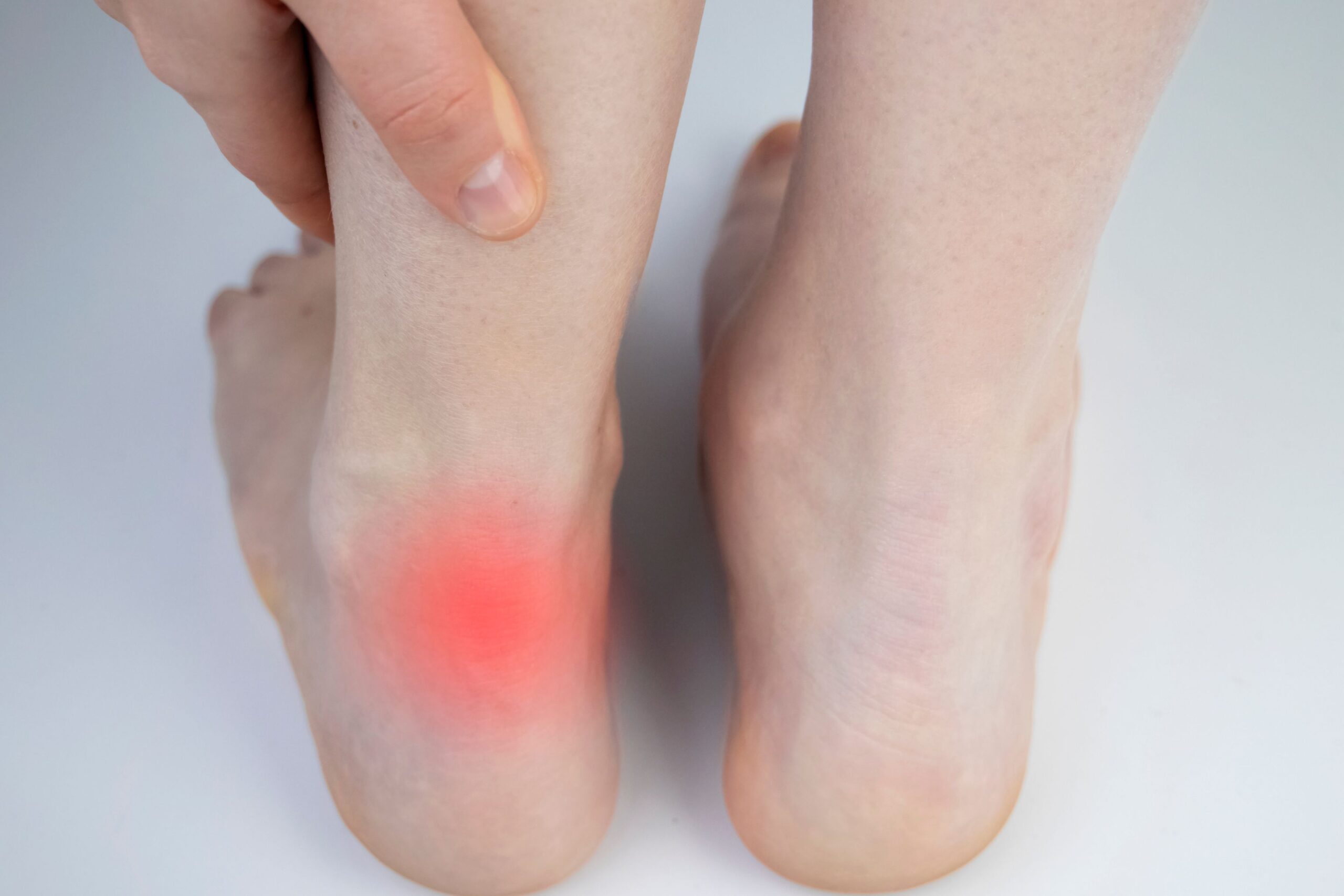
Un problema delle tendinopatie come il tendine d’Achille, il gomito del tennista o la spalla del nuotatore, tra le cause più frequenti di dolore e limitazione funzionale sia nella popolazione generale sia negli atleti, è che sono spesso refrattarie ai trattamenti tradizionali come farmaci antinfiammatori e fisioterapia. Il limite delle strategie terapeutiche è rappresentato dalla ancora incompleta comprensione dei meccanismi molecolari alla base della disorganizzazione della matrice extracellulare e delle alterazioni neurovascolari.
Ora una ricerca coordinata dal Politecnico federale di Zurigo fa un passo avanti, identificando un potenziale interruttore molecolare che innesca la degenerazione dei tendini: si tratta della proteina HIF1α (Fattore Inducibile dall’Ipossia 1α), la cui attivazione è strettamente legata al sovraccarico meccanico cronico. HIF1α regola la risposta delle cellule a condizioni di stress e ipossia, attivando vie genetiche che modificano il metabolismo e la struttura del tessuto.
Oltre che un marcatore, emerge come vero driver causale della tendinopatia. In questo senso, HIF1α si comporta come un vero e proprio “interruttore molecolare” della risposta patologica al sovraccarico e potrebbe rappresentare un nuovo target farmacologico, aprendo nuove prospettive per il trattamento e la prevenzione.
Il trigger molecolare delle tendinopatie: lo studio
I ricercatori hanno condotto esperimenti su modelli animali e su cellule tendinee umane, prelevate da interventi chirurgici sui tendini, analizzando le alterazioni della funzione di questi tessuti in parallelo alle loro caratteristiche genetiche. Nei modelli murini di tendinopatia, hanno attivato la proteina HIF1α – già nota per essere presente a livelli elevati nei tendini malati – in modo permanente o l’hanno disattivata completamente, osservando che l’attivazione di HIF1α risultava sufficiente a indurre tendinopatia anche in assenza di sovraccarico, mentre la sua inibizione ha prevenuto completamente il danno, anche in condizioni di eccessivo carico meccanico.
Sia nei test sui topi sia in quelli su cellule umane è emerso che livelli elevati di proteina HIF1α nel tessuto determinano un rimodellamento alterato dei tendini, con molti legami incrociati (cross-linking) tra le fibre di collagene che li rendono più fragili e ne compromettono la funzione meccanica. In modo sorprendente, questi effetti si verificano indipendentemente da fenomeni di ipervascolarizzazione, suggerendo che le alterazioni strutturali del tessuto siano il vero meccanismo primario della malattia.
Risultati e implicazioni
La ricerca, pubblicata di recente su Science Translational Medicine, non solo identifica il ruolo critico di HIF1α nella malattia dei tendini in risposta al sovraccarico, ma sottolinea anche l’importanza di intervenire precocemente, soprattutto negli atleti più giovani, per prevenire il danno irreversibile innescato dalla proteina. Il lavoro indica che agire nelle fasi iniziali del sovraccarico potrebbe essere cruciale per evitare l’attivazione dei meccanismi degenerativi: «Una volta instaurato, il rimodellamento patologico diventa difficilmente reversibile e la fisioterapia tradizionale non basta più, rendendo necessario il ricorso a interventi chirurgici per rimuovere il tessuto danneggiato», spiegano i ricercatori.
Ora bisognerà indagare l’eventualità di sviluppare farmaci in grado di disattivare la proteina, prevenendo o curando queste patologie, anche se al momento sembra alquanto complesso: HIF1α è, infatti, coinvolta in numerosi processi fisiologici in diversi tessuti, rendendo difficoltoso sviluppare terapie che la colpiscano senza effetti collaterali.
I ricercatori si impegneranno come prima cosa a capire più da vicino quali molecole specifiche del tessuto tendineo sono condizionate da HIF1α: molecole che potrebbero rappresentare potenziali target farmacologici più selettivi e quindi più facilmente utilizzabili a livello clinico.
Moschini G, Mohanan AG, Niewczas IS et al. HIF1α gates tendon response to overload and drives tendinopathy independently of vascular recruitment. Sci Transl Med. 2026 Jan 7;18(831):eadt1228. doi: 10.1126/scitranslmed.adt1228.Epub 2026 Jan 7.